サイケデリック・ルネッサンスから20年が経過したが、神経科学者たちはいまだに、サイケデリックの作用機序や、こうした薬物に関する誤解を正す方法の理解に苦慮している。
1960年代、幻覚剤研究は画期的な進歩を遂げようとしていたと伝えられ、多くの精神疾患を治療できる特効薬と目されていました。研究者たちは、シロシビン(「マジックマッシュルーム」の主成分)やリゼルグ酸ジエチルアミド(LSDまたは「アシッド」)といった薬物が、たった一度の服用で、うつ病、依存症、さらには性機能障害といった深刻な症状から救ってくれる可能性があることを発見しました。1しかし、アメリカ合衆国政府は幻覚剤を個人や社会にとって不安定な脅威とみなし、1970年に規制物質法によって幻覚剤の研究が禁止されました。スケジュールIとは、乱用される可能性が高く、医療用途のない薬物です。
過去20年間は「サイケデリック・ルネッサンス」の時代であり、熱心な使用者や投資家は、これらの薬物は数年分のセラピー効果を数回の高用量の服用で実現できると主張しています。こうした主張を裏付ける証拠もいくつかあります。例えば、100人以上の患者を対象としたこれまでで最大規模のサイケデリック薬物臨床試験では、複数の精神疾患において症状の重症度に有意な改善が見られました。ある研究では、治療抵抗性うつ病の患者に心理的サポートと併用したシロシビンの高用量単回投与により、中用量および極低用量投与と比較して、最大3週間にわたりうつ病の症状が大幅に軽減されたことが分かりました。2同様に、心的外傷後ストレス障害(PTSD)患者を対象とした2つの研究では、3,4-メチレンジオキシメタンフェタミン(MDMA、「エクスタシー」または「モリー」)を3回投与した後、無効プラセボと比較して最大8週間にわたりPTSDの症状が大幅に軽減されたことが分かりました。3,4その他の研究では、依存症、全般性不安障害、強迫性障害、拒食症の治療において有望な初期結果が示されています。5–8実際、FDA は医薬品開発を促進するために、MDMA、シロシビン、LSD に画期的治療薬の指定を与えました。

臨床試験と並行して、基礎研究や動物実験が、幻覚剤の効果の根本的なメカニズムを解明することを目指してきました。分子レベルや細胞レベルの分析では明確な効果が報告されていますが、幻覚剤がどのようにして美しい映像、信念の深遠な変化、高度な知識感覚を生み出すのか、そしてそのような効果が治療効果に本当に必要なのかは、解明が始まったばかりです。9–11これらの薬物は、心と脳の働きを解明するのに役立つ「心の顕微鏡」であると主張する人もいますが、その抑えきれない熱意は、研究者自身が「クールエイドを飲んだ」かのように思わせることもあります。12–15したがって、これらの薬物を冷静に理解することが不可欠です。まずは基本から始めましょう。
サイケデリックスとは何ですか?
精神科医ハンフリー・オズモンドによって造られた「サイケデリック」という用語は、ギリシャ語の「プシュケ」と「デロス」を結合したもので、「精神の顕現」を意味します。サイケデリックは、薬理学的に異なる様々な幻覚剤を広く指しますが、ここでは、サイケデリックとして最も一般的に説明される薬物、すなわちシロシビンやLSDなどの幻覚性セロトニン2A(5-HT 2A)作動薬に限定して定義します。このカテゴリーに属する一般的なサイケデリックには、ペヨーテやサンペドロサボテンに含まれるメスカリンや、アマゾンの醸造酒アヤワスカの主要精神活性成分であるN , N-ジメチルトリプタミン(DMT)などがあります。 MDMAは、幻覚作用がそれほど強くなく、R体エナンチオマーが5-HT 2A受容体に弱く結合することから、サイケデリックスとは別のクラスであるエンパトゲン(共感誘発物質)またはエンタクトゲン(エンタクトゲン)に分類されることがあります。しかし、5-HT 2A拮抗薬との併用はMDMAの主観的および認知的効果を減弱させることから、MDMAは典型的なサイケデリックスと特定のメカニズムを共有している可能性が示唆されています。16,17研究者たちは、MDMAが社会的結びつきや共感の感情を促進するのは、主にノルエピネフリン、ドーパミン、そして特にセロトニンの放出によるものだと考えていますが、アンフェタミンなど、同様の薬理作用を持つ他の精神刺激薬は、これらのエンタクトゲン効果を引き起こしません。
分子レベルで見た幻覚剤の脳への作用メカニズム
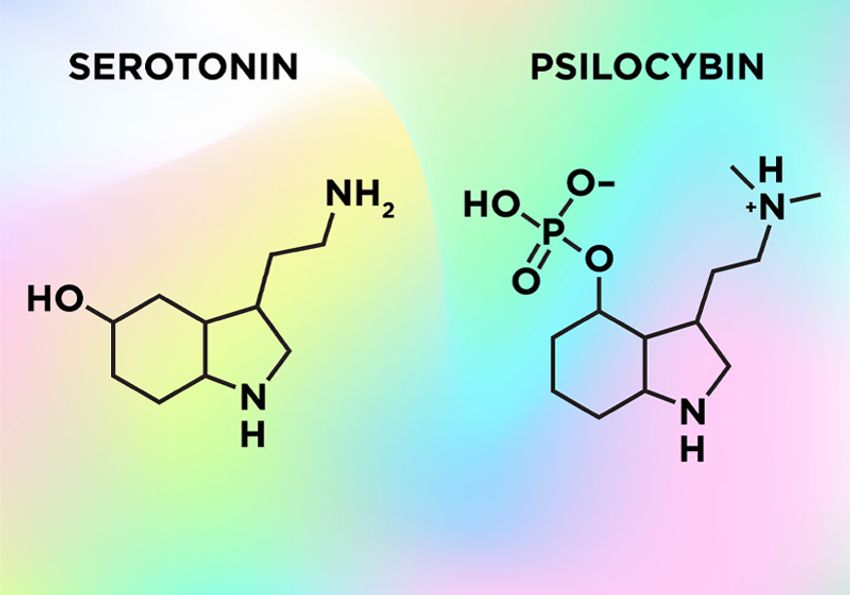
分子薬理学レベルでは、幻覚剤の作用におけるセロトニン経路の重要性については、ある程度の確信が得られています。幻覚剤治療の対象となる疾患は、一般的にセロトニン経路に作用するFDA承認の薬剤で治療されていることを考えると、これは驚くべきことではないかもしれません。シロシビン、LSD、メスカリン、DMT、そして同様の主観的効果を持つあまり知られていない幻覚剤はすべて、5-HT 2A受容体の作動薬であり、多くの幻覚剤の化学構造はセロトニンに類似しています。他のセロトニン受容体サブタイプ(例えば、5-HT 1Aや 5-HT 2C )も、様々な幻覚剤の作用において無視できない役割を果たしている可能性がありますが、幻覚剤の5-HT 2A受容体への親和性は、その効力と密接に関連しています。18実際に、5-HT 2A受容体を阻害すると、主観的な効果の大部分が抑制され、すでに始まっている「トリップ」を中断させることさえできる。19,20
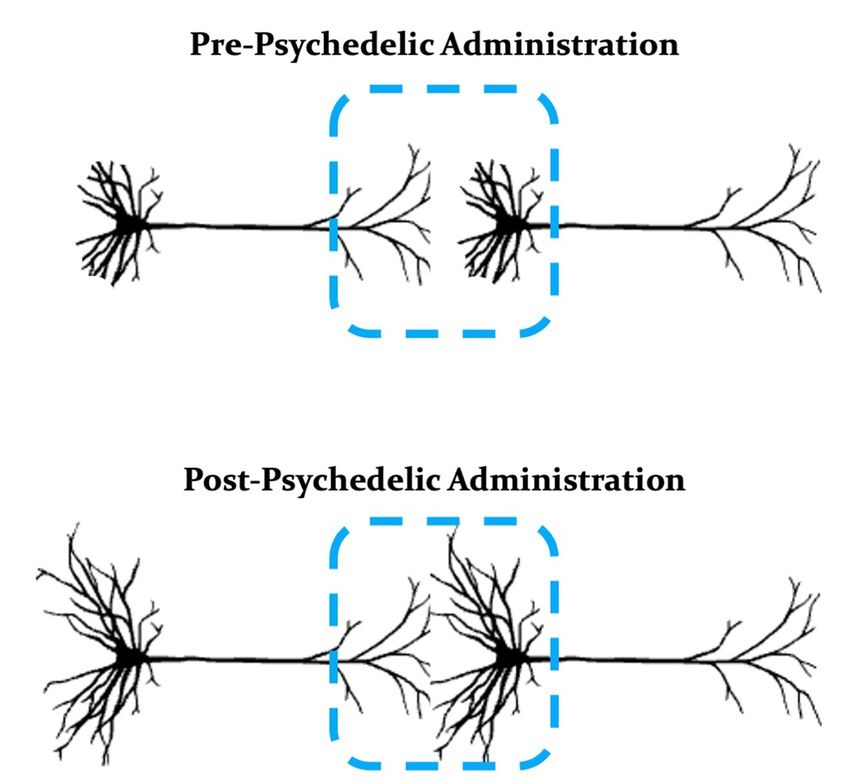
細胞神経科学者たちは最近、サイケデリック薬が神経可塑性を高めるという仮説を提唱している。これは様々な神経変化、特にシナプスで起こる変化を指す。研究者たちは、可塑性が様々な学習や記憶の基盤であり、様々な精神疾患で障害されていると考えている。21サイケデリック薬による可塑性の主な証拠は、樹状突起形成(樹状突起の成長)と棘突起形成(シナプスの特定の部位である樹状突起上の突起であるスパインの成長)の促進から得られている。動物モデルにおいて、サイケデリック薬の単回投与は樹状突起と棘の数を増加させることが報告されている。22これらの効果は投与後数時間以内に発現し、その後数日かけて増強し、最大1ヶ月間持続することがある。23
サイケデリック薬は、長期増強(あるニューロンが他のニューロンに与える影響を強める)の誘導など、他の形態の可塑性も促進する可能性があります。24,25 サイケデリック薬は、5 -HT 2A受容体が密集している皮質錐体細胞(主要な興奮性ニューロン)において、複数の可塑性マーカーを確実に誘導しますが、5-HT 2Aの発現が低く、主に抑制性介在ニューロンに限定されている海馬では、このような増強は一貫性がなく、減少として観察されることもあります。26–28 同様に、サイケデリック薬が海馬における神経新生(新しいニューロンの成長)を増加させると報告した科学者もいますが、反対の結果を得た科学者もいます。27
サイケデリック薬が特定の形態の可塑性を高めるとしても、可塑性が高まることが必ずしも有益とは限らない。アンフェタミンなどの精神刺激薬も構造的シナプス可塑性を高めるが、これらの効果には複数回の投与が必要であり、線条体などの他の領域にも影響を及ぼす可能性がある。29一部の研究者は、報酬と空間学習に関連する脳構造である線条体と海馬における可塑性の誘導には、サイケデリック薬投与後の数日間の「臨界期」における特定の環境入力が、これらの構造とそれらが支える行動に変化をもたらすために必要となる可能性があることを発見している。30,31これまでのところ、サイケデリック薬が言語学習などの人間特有の臨界期を活性化させることは研究者によって発見されていないが、サイケデリック体験は人を「子供のような」状態に再びさせると逸話的に説明されている。しかし、動物モデルにおける可塑性を促進する体重ベースの投与量は、人間が通常摂取する量よりも桁違いに大きく、これらの研究結果の一般化には疑問が残る。
幻覚作用のメカニズムを理解するためのシステムと認知神経科学モデルアプローチ
5-HT 2A の活性化が、幻覚剤による知覚の歪みにどのようにつながるのかは依然として不明である。さらに、神経可塑性に関する多くの指標はヒトにおいて容易に測定できないため、可塑性の向上と精神的健康の改善との関係は曖昧になっている。このような高次の現象を理解するために、研究者たちはシステムレベルおよび認知レベルのアプローチを用いて脳機能を調べてきた。多くの場合、彼らは機能的磁気共鳴画像法(fMRI)を用いて血中酸素化(神経活動の代理指標)の局所的な変化を測定し、幻覚剤がヒトの脳回路やネットワークに及ぼす急性および後急性の影響を調査している。しかし、これらの影響の多くは再現できず、特に後急性の薬物影響は再現性がない。32そのため、本稿では主に急性影響について議論する。
視床ゲーティングモデル
幻覚剤の作用に関する初期の回路モデルである視床ゲーティングモデルでは、幻覚剤が視床による感覚フィルタリングを弱めると提唱されている。33皮質の5-HT 2A発現興奮性ニューロンを活性化することで、これらのニューロンは線条体の抑制性ニューロンを活性化し、線条体は淡蒼球の抑制性ニューロンを抑制するため、視床の抑制が解除される。神経科学者は、この視床の「脱抑制」によって皮質が感覚情報で溢れ、知覚の歪み、注意散漫の増大、知覚による制御の圧倒的な喪失につながる正のフィードバックループが形成されると理論づけている。いくつかの fMRI 研究では、幻覚剤がタスクフリー(すなわち「安静状態」)の条件下で視床と皮質間の脳活動のカップリング(すなわち「機能的連結性」)を高めることが明らかになっている。34–37さらに、動物およびヒトの研究では、急性サイケデリック効果下では感覚フィルタリングが損なわれることが示唆されている。サイケデリックの急性効果の間、げっ歯類の聴覚ニューロンは馴染みのある刺激への反応を減衰させることができず、ヒトおよび動物の両方の研究で、大きな音に対する驚愕反応が、その前により小さな音があると減衰するときに起こる感覚フィルタリングプロセスであるプレパルス抑制の減少が見られている。38–40しかし、2つの音の間の遅延が大きい場合、サイケデリックはプレパルス抑制に影響を与えないか、むしろ強化する可能性がある。41,42また、視床ゲーティングモデルがサイケデリックの持続的な治療効果とどのように関連しているかは不明である。
人気があるが、問題のある反証不可能なモデル:REBUS
近年注目を集めているもう一つのモデルは、サイケデリック薬物依存のRElaxed Beliefs Under pSychedelics(REBUS)です。43 REBUSは、社会的処理、自己関連処理、エピソード記憶、意味記憶など、幅広い認知機能を支える標準的な大規模皮質ネットワークであるデフォルトモードネットワーク(DMN)に焦点を当てています。44 REBUSは、個人が安静状態にあるときに特に活発に活動するDMNが脳の情報処理階層の最上位に位置し、サイケデリック薬物がDMNの機能を弱めることでこの階層を混乱させると仮定しています。いくつかの研究で、サイケデリック薬物がDMNの領域間の(安静時の)機能的接続を弱めることが明らかになっています。45–50 DMNが高次の信念表象(すなわち、必ずしも他者と共有されていない意味記憶)において果たす役割を考慮すると、科学者たちは、サイケデリック薬がDMNの機能的結合性に及ぼす影響は、世界についての人々の想定を緩め、それによって不確実性と新奇性の知覚を増加させると考えています。DMNが自己関連処理において果たす役割を踏まえ、研究者たちは、DMN機能の減衰が「自我の崩壊」、つまりサイケデリック薬の変動的な効果(一時的に自己意識が失われる)を引き起こすと仮説を立てています。最後に、脳の階層構造の最上位(下位レベルの活動を制限するとされる)を乱すことで、エントロピーと信号圧縮率の指標で表される神経活動がより複雑になり、脳ネットワーク内のコミュニケーションの減少とネットワーク間のコミュニケーションの増加を含む、より多様な脳状態につながる可能性があると研究者たちは考えています。これらの効果は、環境からの低レベルの感覚情報に対する感受性を高め、不適応的な信念の修正を可能にすると考えられています。例えば、うつ病やPTSDに長年苦しんだ後、自分は良い人間ではない、あるいは世界は危険だといった不適応的な信念を抱いてしまうことがあります。そのため、そのような信念を「アンラーニング(忘れること)」することは、治療効果をもたらす可能性があります。
REBUS理論の大きな問題は、反証可能性の欠如です。ある考えが反証可能であるとは、その考えが誤りであることを証明できる証拠を思いつくことができる場合です。もしある理論が、理解可能な矛盾を一切回避できる場合、それは通常、科学の領域外、あるいは少なくとも検証する価値のある領域外とみなされます。REBUS理論は主に自由エネルギー原理に基づいており、議論の多い意識理論である統合情報理論と類似点があります。51,52自由エネルギー原理と統合情報理論はどちらも反証不可能と考えられており、したがって、REBUS理論の特定の主張もまた、概ね反証不可能です。53,54
REBUSが取り組むべき、より具体的な問題もいくつかある。第一に、幻覚剤は逆説的に親近感を生み出し、誤った信念の可能性を含め、信念を強化する可能性がある。10,55第二に、幻覚効果を媒介するDMNの特異性は疑問視されている。ある研究では、DMNの機能的連結性の減衰が自我の崩壊と関連していることが示されたが、より質の高いデータを用いた再現実験では、相関はほぼゼロであることがわかった。35,46さらに、アルコール、大麻、コーヒー、アンフェタミン、さらには抗うつ薬セルトラリンの非精神活性単回投与など、他の薬物もDMNの機能的連結性を急激に減衰させることが分かっている。56–60対照的に、幻覚剤と頻繁に比較され、うつ病の治療に広く使用されている(S鏡像異性体はFDA承認されているものの、大部分は適応外である)薬理学的に異なる解離性薬物であるケタミンは、DMN内の機能的連結性を低下させる、効果がない、または増加することが判明している。61–66幻覚剤のDMN連結性に対する急性期後の影響も大きく一貫性がなく、分析方法に応じて、同じデータセットで効果なし、増加、減少、またはその両方が見られる研究もある。49,67–73 500人以上の参加者を対象とした研究では、うつ病においてDMN機能的連結性の増加と減少の両方が見られ、この指標がうつ病の有用なバイオマーカーとして疑問視されている。74,75以下を読み続けてください…
サイケデリック薬によって生じる神経複雑性の増大はシナプス可塑性の増加と関連していると推測したくなるかもしれないが、神経複雑性の増大は急性期の薬物効果時に最も顕著であり、急性期後には一貫して認められない。対照的に、可塑性の増加は急性期後に顕著になる。これらの神経複雑性の増大は、必ずしもサイケデリック薬によって促進される特有の認知活動を示すものではなく、むしろ安静時神経画像法の使用によるアーティファクトである可能性もある。薬物を投与しない状態でスキャナー内で休息するよう指示された場合、認知活動の配列は最小限に抑えられ、主に空想などの内的思考に集中する可能性が高い。さらに、参加者の40%以上が(薬物を投与しない)安静時に眠りに落ち、睡眠は神経複雑性の低下と関連している。76,77内的思考を促進する条件はDMN活動も促進するため、安静時に観察されるDMN活動レベルが高く、環境への注意を向けることでDMN活動が弱まる可能性がある。サイケデリック薬の急性効果は睡眠を妨げるため、スキャナーの音に注意を向けたり、目を開閉したり、将来の計画について考えたりするなど、外的注意と内的思考の両方に焦点を当てた、より広範な認知操作が促進されます。しかし、これらの認知操作はどれもサイケデリック体験に特有のものではありません。したがって、薬物を投与されていない状態で参加者に様々な認知操作を行わせるだけでも、神経複雑性は増加するはずです。実際、2つの研究では、参加者に薬物を投与されていない状態で複雑な認知操作(知覚課題や映画鑑賞など)を行わせると、安静時と比較して神経複雑性が増加しただけでなく、この複雑性の増加は、安静時のサイケデリック薬投与、あるいは同じ認知操作を行った場合の複雑性の増加と同程度に達することが明らかになっています。49,78サイケデリック薬投与下で比較的退屈な課題に取り組むことは、サイケデリック体験から離脱することで神経複雑性を弱める可能性さえあります(「グラウンディング」として知られています)。しかし、幻覚剤投与下でこれらの課題を実行すると、神経複雑性が増大する傾向もありました。もし神経複雑性が特有の幻覚効果を指標としているのであれば、薬物非投与下で課題指向的な認知操作を行っても、幻覚効果レベルの神経複雑性に達することは決してないはずです。幻覚剤の作用に関する包括的なシステムレベルモデルは、様々な状況下で幻覚効果を捉えることができ、課題操作の導入に対してそれほど脆弱ではないはずです。
とても新しいのにとても馴染み深い:サイケデリック、記憶、そして信念の変化
我々の研究グループは最近、幻覚剤の作用に関する包括的なモデルではなく、特に可塑性が記憶の獲得と更新を支えていると考えられていることを踏まえ、幻覚剤が様々な学習・記憶システムに及ぼす影響に焦点を当てています。幻覚体験から得られるもの、つまり記憶は、これらの薬物が精神的健康に及ぼす持続的な影響を説明する上で大きな価値を持つ可能性があります。例えば、いくつかの研究では、幻覚剤の急性効果と急性期後効果が、条件付けされた恐怖の消去学習を増強できることが示されています。79消去学習は、以前は嫌悪的な結果(例えばショック)と関連していた刺激(例えば音)が、嫌悪的な結果を伴わずに複数回提示されたときに発生し、その刺激がもはや脅威を予兆しないという新たな学習につながります。消去学習は、PTSDの症状を軽減するために患者がトラウマ記憶に繰り返し直面する曝露療法など、行動療法の有用な実験モデルと考えられています。残念ながら、恐怖は消去後にすぐに再発する可能性があるため、幻覚剤を使用して消去学習を強化すると、曝露に基づく治療の有効性が向上する可能性があります。

サイケデリック薬はすべての学習プロセスを強化するわけではなく、特定の学習形態を阻害することさえありますが、こうした相反する効果は必ずしも有害とは限りません。サイケデリック薬は認知柔軟性、つまり変化する環境に直面した際に認知操作を切り替える能力を高めるという仮説が一般的です。対照的に、サイケデリック薬の急性効果と急性後効果は、認知柔軟性の指標を阻害する効果と向上させる効果の両方を持つことが分かっており、これは学習プロセスへの相反する効果によって説明できる可能性があります。67,80–83最も印象的な発見の一つは、サイケデリック薬が海馬と大脳皮質によって支えられる記憶の形成に異なる影響を与えるという点です。アルコール、ケタミン、大麻など、抑制や長期増強の障害を促進する向精神薬と同様に、サイケデリック薬の急性効果は海馬依存性エピソード記憶の形成を確実に阻害します。これは、海馬の抑制性ニューロンにおける5-HT 2Aの顕著な発現と一致しています。 84これらの他の薬物とは対照的に、また皮質の5-HT 2Aを発現する興奮性ニューロンと一致して、我々は 3 つの別々の研究で、サイケデリック薬が、親しみやすさと呼ばれる皮質依存性記憶の形成を特異的に回避、あるいは促進することを発見した。84,85 親しみやすさは、特定の詳細を必ずしも思い出さなくても、刺激を最近経験したことを知っているときに生じる。例えば、いつどこでその人に会ったかを覚えていなくても、顔を認識するなどである。一つの説明として、サイケデリック薬は、与えられた刺激に対する当初の知覚された新奇性とその後の情報処理を高めるが、より高度な情報処理は、その後の親しみやすさを高める、というものがある。このような説明は、サイケデリック薬によってもたらされる新奇性と親しみやすさの両方の逆説的な高まりを説明できるかもしれない。急性サイケデリック効果下におけるこの皮質優位の情報処理モードは、急性効果後の皮質可塑性の向上と相まって、通常は数ヶ月から数年かけて形成される新たな意味記憶の具体化を加速させ、結晶化した不適応的信念を崩壊させる可能性がある。実際、マウスにおいて皮質可塑性を人工的に高めることで、意味記憶のような記憶を崩壊させることができる。86しかし、親近感の高まりは、知覚されているものの錯覚的な真実をも引き起こす可能性があり、これは錯覚的真実効果として知られる現象である。87この仮説が正しいとすれば、誤った信念の誘発を避けながら、特定の不適応的信念をどのように置き換えるかに焦点を当てる必要がある。

サイケデリック研究における複雑さの単純な真実
サイケデリック薬の治療効果を検証する臨床試験は、主に標準的な心理的支援プロトコルに従って行われてきた。準備セッションでは患者がセラピストと信頼関係を築き、投与セッションでは参加者は薬物を摂取し、アイシェードを装着して音楽を聴きながらソファに横たわり、統合セッションでは参加者が投与セッションの体験についてセラピストと話し合う。この心理的支援モデルは最近まで、「サイケデリック補助療法」の治療効果に不可欠であると考えられてきた。しかし、これらの試験に組み込まれている心理的支援は適切に標準化されておらず、単独の治療として有効であることが示されておらず、サイケデリック薬投与の治療効果に対する重要な寄与因子として実証的に検証されたこともない。88,89このことから、この「ソファ方式」が最大の治療効果をもたらす投与セッションにおける最良の方法なのかどうかという疑問が生じる。79さらに、一部の研究では、実薬群で観察された自殺念慮の発現率の高さなど、有害事象の発生率と重症度の評価が軽視されている。こうした制約やその他の制約が、FDAがPTSD治療におけるMDMA補助療法を却下した一因となっている可能性がある。この療法は、目覚ましい有効性データにもかかわらず、新薬申請段階に達した最初のサイケデリック療法パッケージである。サイケデリックの急性および急性期後効果の根底にある基本的なメカニズムを理解することは、これらの薬物のメリットを最大化し、害を最小限に抑える心理療法の条件や種類を明確にするのに役立つ可能性がある。
まとめると、大衆メディアによって煽り立てられたサイケデリック薬の継続的な誇大宣伝、すなわちこれらの薬物の万能薬的な性質と、その害悪を誇張したプロパガンダキャンペーンには、引き続き警戒を怠ってはならない。また、サイケデリック薬の作用機序について、こうした偏見を強調する過度に単純化された説明にも警戒しなければならない。実際、幅広い精神疾患を治療し、信念を緩和・強化し、目新しさと親しみやすさを生み出し、認知の柔軟性を低下・強化し、記憶を低下・強化する薬物は、単純な説明では説明できない可能性が高い。
開示情報: MKDはVCENNAの顧問です。GAFはSynapseBio AIのコンサルタントを務め、Alto Neuroscienceの株主でもあります。CBNは、Engrail Therapeutics、Clexio Biosciences LTD、Sero(旧Galen Mental Health LLC)、Goodcap Pharmaceuticals、Sage Therapeutics、Senseye Inc、Precisement Health、Autobahn Therapeutics Inc、EMA Wellness、Denovo Biopharma LLC、Alvogen、Acadia Pharmaceuticals、Inc、Reunion Neuroscience、Kivira Health、Inc、Wave Neuroscience、Patient Square Capital LP、Invisalert Solutions Inc.、およびNeurocrine Biosciences、LLCのコンサルタントです。 CBNは以下の特許を保有しています:リチウムの経皮投与方法およびデバイス(US 6,375,990B1)、モノアミン神経伝達物質の輸送阻害を介した抗うつ薬療法の評価方法(ex vivoアッセイ)(US 7,148,027B2)、化合物、組成物、合成方法、および治療法(CRF受容体結合リガンド)(US 8,551,996 B2)。CBNは、Corcept Therapeutics Company、EMA Wellness、Precisement Health、Signant Health、Galen Mental Health LLC、Kivira Health, Inc.、Denovo Biopharma LLC、およびSenseye Inc.の株式を保有しています。これらのグループはいずれも、本記事の執筆に関与していません。
Reference : How Psychedelics Affect the Brain: What We Know, and What We Think We Know
https://www.the-scientist.com/how-psychedelics-affect-the-brain-what-we-know-and-what-we-think-we-know-73516